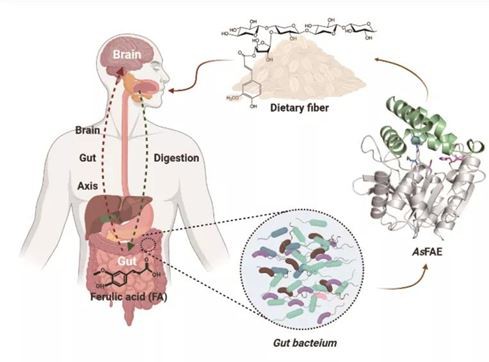
اخیرا، تیم نوآوری مهندسی آنزیم غذایی مؤسسه فرآوری محصولات کشاورزی، آکادمی علوم کشاورزی چین نوع جدیدی ازاسید فرولیکاستراز به عنوان FAE از Allobacterium serratia روده مکانیزم های اتصال و کاتالیزوری یک پایه علمی برای درک عمیق مکانیسم متابولیسم فیبر غذایی در دستگاه روده و همچنین راهنمایی برای تغذیه دقیق و تنظیم دقیق پزشکی آنزیم های روده فراهم می کند. نتایج تحقیق مرتبط در مجله شیمی کشاورزی و مواد غذایی در قالب یک مقاله روی جلد با عنوان"The α-Helical Cap Domain of a Novel Esterase from Gut Alistipes shahii Shaping the Substrate-Binding Pocket [ GG] quot;.
به گفته محقق Xin Fengjiao، فلور روده انسان پل اصلی است که متابولیسم غذا و تنظیم تغذیه بدن را به هم متصل می کند و نقشی حیاتی در سلامت و بیماری انسان ایفا می کند. فلور خاص می تواند با رمزگذاری فرولیک اسید استراز خاص، اسید فرولیک عملکردی را از فیبر غذایی آزاد کند و سپس عملکردهایی مانند ضد اکسیداسیون، ضد عفونت، ضد تومور، بهبود بیماری های قلبی عروقی و تنظیم شناخت مغز را اعمال کند. در مطالعه قبلی، هفت ژن فرولیک اسید استراز با استفاده از تخمیر باکتریهای مدفوع آزمایشگاهی تنظیم شدند. در این مطالعه، بیان، خالصسازی و خواص آنزیمی فرولیک اسید استراز مشتق شده از باکتری S. روده انجام شد. دمای بهینه آنزیم 40 درجه سانتیگراد، pH مطلوب 8.5 است و ترجیح سوبسترای بالایی برای استرهای اسید چرب با زنجیره کوتاه دارد. این مطالعه ساختار سه بعدی آنزیم را بیشتر تجزیه و تحلیل کرد و نشان داد که"cap" دامنه نقش مهمی در اتصال و کاتالیز سوبسترای آنزیم' ایفا می کند.